摘要
鋰離子電池中極片殘留水分測(cè)試及所帶來(lái)的影響
內(nèi)容
1、水分危害電池性能的基本機(jī)理
鋰離子電池中水分如果過(guò)高��,會(huì)與電解液反應(yīng)����。首先,水分與電解液里面的鋰鹽反應(yīng)生成HF:
H2O+LiPF6→POF3+LiF+2HF
氫氟酸是一中腐蝕性很強(qiáng)的酸�,它可以使電池內(nèi)部的金屬零件腐蝕���,進(jìn)而使電池最終漏液��。而且HF破壞SEI膜�,會(huì)與SEI膜主要成分繼續(xù)發(fā)生反應(yīng):
ROCO2Li+HF→ROCO2H+LiF
Li2CO3+2HF→H2CO3+2LiF
最后��,在電池內(nèi)部產(chǎn)生LiF沉淀����,使鋰離子在電池負(fù)極片發(fā)生不可逆轉(zhuǎn)的化學(xué)反應(yīng),消耗活性鋰離子��,電池的能量就減少了�����。當(dāng)水分足夠多時(shí),產(chǎn)生的氣體多����,電池內(nèi)部的壓力就會(huì)變大,從而引起電池受力變形����,出現(xiàn)電池鼓漲,漏液等危險(xiǎn)��。
2��、極片殘留水分測(cè)試
電池極片中殘留的水分一般為幾百ppm����,相對(duì)而言水分含量較低,無(wú)法用簡(jiǎn)單方法測(cè)量����,一般采用卡爾費(fèi)休庫(kù)倫法測(cè)試微量水分,其原理是一種電化學(xué)方法��。儀器電解池中的卡氏試劑達(dá)到平衡時(shí)注入含水的樣品��,水參與碘���、二氧化硫的氧化還原反應(yīng)��,在吡啶和甲醇存在的情況下����,生成氫碘酸吡啶和甲基硫酸吡啶,消耗了的碘在陽(yáng)極電解產(chǎn)生����,從而使氧化還原反應(yīng)不斷進(jìn)行,直至水分全部耗盡為止����,依據(jù)法拉第電解定律����,電解產(chǎn)生的碘同電解時(shí)耗用的電量成正比例關(guān)系的,其反應(yīng)如下:
H2O+I2+SO2+3C5H5N→2C5H5N·HI+C5H5N·SO3
在電解過(guò)程中���,電極反應(yīng)如下:
陽(yáng)極:2I--2e→I2
陰極:I2+2e→2I-
2H++2e→H2↑
從以上反應(yīng)中可以看出�,即1摩爾的碘氧化1摩爾的二氧化硫����,需要1摩爾的水����。所以電解碘的電量相當(dāng)于電解水的電量�,電解1摩爾碘需要2×96493庫(kù)侖電量,電解1毫摩爾水需要電量為96493毫庫(kù)侖電量�。樣品中水分含量根據(jù)式(1)計(jì)算:
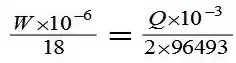
式中:W---樣品中的水分含量,μg���;Q---電解電量��,mC���;18---水的分子量。
卡爾費(fèi)休微量水分測(cè)試儀一般結(jié)構(gòu)如圖1所示��,主要包含卡爾費(fèi)休電解池和卡氏加熱爐����,極片樣品放入密封樣品瓶中,然后一定溫度下加熱樣品瓶�����,樣品中的水分蒸發(fā),然后利用干燥氣體將水蒸氣送入電解池中參與反應(yīng)�,再測(cè)定電解過(guò)程中的電量,從而滴定水分含量�。
相關(guān)資料